يشير الكربون المنشط (AC) إلى المواد عالية الكربون ذات المسامية العالية وقدرة الامتصاص الكبيرة، والتي تُنتج من الخشب وقشور جوز الهند والفحم والمخاريط وغيرها. يُعد الكربون المنشط من أكثر المواد الماصة استخدامًا في مختلف الصناعات لإزالة العديد من الملوثات من المياه والهواء. ونظرًا لتصنيعه من المنتجات الزراعية والنفايات، فقد أثبت الكربون المنشط أنه بديل ممتاز للمصادر التقليدية غير المتجددة والمكلفة. يُستخدم في تحضير الكربون المنشط عمليتان أساسيتان: التفحيم والتنشيط. في العملية الأولى، تُعرَّض المواد الأولية لدرجات حرارة عالية تتراوح بين 400 و850 درجة مئوية، لإزالة جميع المكونات المتطايرة. تعمل درجة الحرارة المرتفعة على إزالة جميع المكونات غير الكربونية من المادة الأولية، مثل الهيدروجين والأكسجين والنيتروجين، على شكل غازات وقطران. تُنتج هذه العملية فحمًا ذا محتوى كربوني عالٍ ولكن بمساحة سطحية ومسامية منخفضة. أما الخطوة الثانية، فتتضمن تنشيط الفحم المُصنّع مسبقًا. يمكن تصنيف تحسين حجم المسام أثناء عملية التنشيط إلى ثلاثة أنواع: فتح المسام التي لم يكن من الممكن الوصول إليها سابقًا، وتطوير مسام جديدة عن طريق التنشيط الانتقائي، وتوسيع المسام الموجودة.
عادةً ما تُستخدم طريقتان للتنشيط، الفيزيائية والكيميائية، للحصول على مساحة سطح ومسامية مرغوبة. يتضمن التنشيط الفيزيائي تنشيط الفحم المتفحم باستخدام غازات مؤكسدة مثل الهواء وثاني أكسيد الكربون والبخار عند درجات حرارة عالية (بين 650 و900 درجة مئوية). يُفضل استخدام ثاني أكسيد الكربون عادةً لنقائه وسهولة التعامل معه وإمكانية التحكم في عملية التنشيط عند حوالي 800 درجة مئوية. يمكن الحصول على تجانس عالٍ للمسام باستخدام ثاني أكسيد الكربون مقارنةً بالبخار. مع ذلك، يُفضل استخدام البخار في التنشيط الفيزيائي نظرًا لإمكانية إنتاج فحم منشط بمساحة سطح عالية نسبيًا. وبسبب صغر حجم جزيئات الماء، ينتشر بكفاءة داخل بنية الفحم. وقد وُجد أن التنشيط بالبخار أعلى بنحو ضعفين إلى ثلاثة أضعاف من التنشيط بثاني أكسيد الكربون عند نفس درجة التحويل.
مع ذلك، تتضمن الطريقة الكيميائية مزج المادة الأولية مع عوامل التنشيط (مثل هيدروكسيد الصوديوم، وهيدروكسيد البوتاسيوم، وكلوريد الحديد الثلاثي). تعمل هذه العوامل كمؤكسدات ومجففات في آنٍ واحد. في هذه الطريقة، تتم عمليتا التفحيم والتنشيط معًا عند درجة حرارة منخفضة نسبيًا (300-500 درجة مئوية) مقارنةً بالطريقة الفيزيائية. ونتيجةً لذلك، يؤثر ذلك على التحلل الحراري، مما يؤدي إلى تمدد بنية مسامية محسّنة وزيادة إنتاج الكربون. من أهم مزايا الطريقة الكيميائية مقارنةً بالطريقة الفيزيائية: انخفاض درجة الحرارة المطلوبة، وبنية مسامية دقيقة عالية، ومساحة سطح كبيرة، وتقليل زمن اكتمال التفاعل.
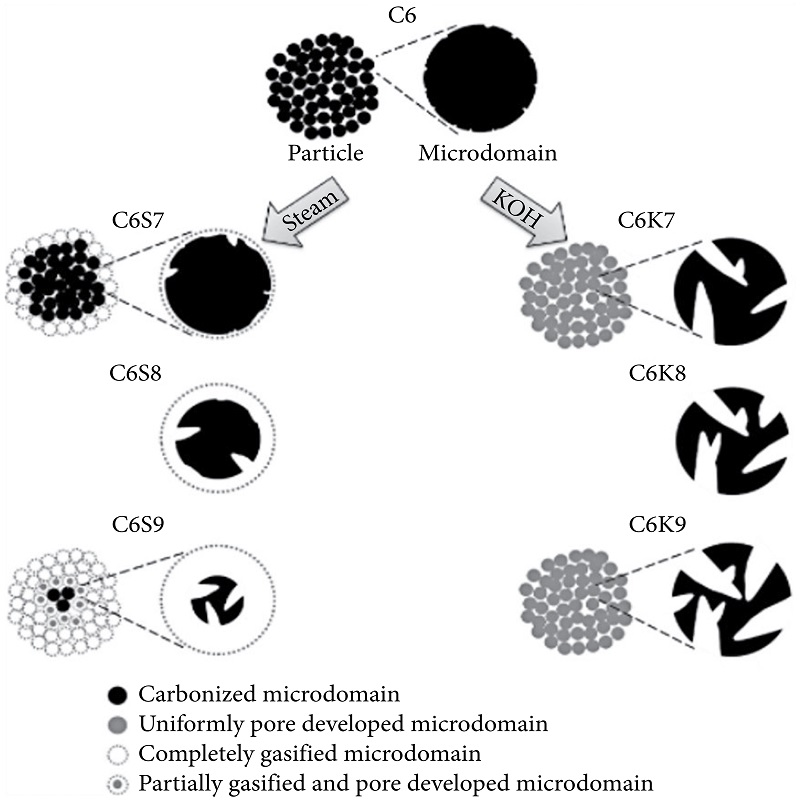
يمكن تفسير تفوق طريقة التنشيط الكيميائي استنادًا إلى نموذج اقترحه كيم وزملاؤه [1]، والذي يُشير إلى وجود نطاقات مجهرية كروية متعددة مسؤولة عن تكوين المسام الدقيقة في الكربون المنشط. في المقابل، تتشكل المسام المتوسطة في المناطق الواقعة بين النطاقات المجهرية. عمليًا، قاموا بتكوين الكربون المنشط من راتنج أساسه الفينول عن طريق التنشيط الكيميائي (باستخدام هيدروكسيد البوتاسيوم) والتنشيط الفيزيائي (باستخدام البخار) (الشكل 1). أظهرت النتائج أن الكربون المنشط المُصنّع بالتنشيط باستخدام هيدروكسيد البوتاسيوم يتميز بمساحة سطحية عالية تبلغ 2878 م²/غ، مقارنةً بـ 2213 م²/غ المُصنّع بالتنشيط باستخدام البخار. بالإضافة إلى ذلك، وُجد أن عوامل أخرى، مثل حجم المسام، ومساحة السطح، وحجم المسام الدقيقة، ومتوسط عرض المسام، كانت جميعها أفضل في ظروف التنشيط باستخدام هيدروكسيد البوتاسيوم مقارنةً بالتنشيط باستخدام البخار.
تم شرح الاختلافات بين الكربون المنشط المحضر من التنشيط بالبخار (C6S9) والتنشيط بهيدروكسيد البوتاسيوم (C6K9)، على التوالي، من حيث نموذج البنية المجهرية.
بحسب حجم الجسيمات وطريقة التحضير، يمكن تصنيف الكربون المنشط إلى ثلاثة أنواع: الكربون المنشط المسحوق، والكربون المنشط الحبيبي، والكربون المنشط الخرزي. يتكون الكربون المنشط المسحوق من حبيبات دقيقة بحجم 1 مم، بمتوسط قطر يتراوح بين 0.15 و0.25 مم. أما الكربون المنشط الحبيبي، فيتميز بحجم أكبر نسبيًا ومساحة سطح خارجية أصغر. ويُستخدم الكربون المنشط الحبيبي في تطبيقات متنوعة في الطورين السائل والغازي، وذلك تبعًا لنسب أبعاده. النوع الثالث: الكربون المنشط الخرزي، يُصنع عادةً من قطران البترول، ويتراوح قطره بين 0.35 و0.8 مم. ويُعرف بقوته الميكانيكية العالية ومحتواه المنخفض من الغبار. ويُستخدم على نطاق واسع في تطبيقات الطبقة المميعة، مثل ترشيح المياه، نظرًا لبنيته الكروية.
تاريخ النشر: 18 يونيو 2022

